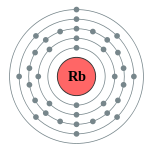
铷
原子序數為37的化學元素
德國化學家羅伯特·威廉·本生和古斯塔夫·基爾霍夫於1861年利用當時的新技術火焰光譜法發現了銣元素。其名稱rubidium源自拉丁語rubidus,意為深紅色,是銣元素發射光譜之特徵譜線的顏色。
儘管地殼中銣的含量比銫豐富得多,甚至超過銅等常見金屬,但銣分佈稀散,本身沒有獨立礦床,主要為開採鋰和銫的副產品產出,且年產量非常有限。產能的限制使得銣化合物價格昂貴,再加上性質相似的銫比銣具有更強的電正性,故產業上銫的應用領域比銣更加廣泛。銣化合物主要用於化學和電子範疇的研究和開發,銣也被用於高精度原子鐘、特種玻璃、催化劑等領域[4]。此外,銣金屬能夠輕易氣化,而且它有特殊的吸收光譜範圍,所以常被用在原子的雷射操控技術上。
銣沒有已知的生理功用,但生物體對銣離子的處理機制和鉀離子相似,因此銣離子會被主動運輸到植物和動物細胞中。銣的化學毒性很低,有研究顯示將生物體中少部分的鉀離子替換為銣離子並不會產生任何顯著的負面影響。不過銣金屬會和水發生爆炸性的劇烈反應,能夠引發火災,故屬於危險化學品。
歷史编辑

1861年,羅伯特·威廉·本生和古斯塔夫·基爾霍夫在德國海德堡,利用光譜儀在鋰雲母中發現了銣元素。由於其發射光譜呈現出多條鮮明的紅線,所以他們選擇了拉丁文中意為「深紅色」的「rubidus」一詞為它命名。[5][6]
銣是鋰雲母中的一種次要成分。基爾霍夫和本生所處理的150公斤鋰雲母中,只含有0.24%的氧化銣(Rb2O)。鉀和銣都會和氯鉑酸形成不可溶鹽,但在熱水中,兩種鹽的可溶性有小許差異。可溶性稍低的六氯鉑酸銣(Rb2PtCl6)可以經分級結晶的方法取得。用氫對六氯鉑酸銣進行還原後,基爾霍夫和本生獲得了0.51克的氯化銣。兩人之後對銣和銫進行的首次大型萃取工序用到了4萬4千升礦物水,並一共提取出7.3克氯化銫和9.2克氯化銣。[5][6]基爾霍夫和本生在發明光譜儀僅僅一年後就發現了銣元素。銣因此成為繼銫以後第二個通過光譜學方法發現的元素。[7]
兩人用提取出的氯化銣來估計銣的原子量,得出的數值為85.36(目前受認可的數值為85.47)。[5]他們試圖對熔融氯化銣進行電解以取得單質銣,但他們取得了一種藍色的均勻物質,且「無論在肉眼還是顯微鏡下都無法看出絲毫的金屬成分」。他們推測這種物質是低價氯化銣(Rb
2Cl),不過它其實更可能是銣金屬和氯化銣的膠體狀混合物。[8]之後,本生進行了第二次嘗試,對炭化了的酒石酸銣加熱,成功還原了銣金屬。儘管蒸餾出的銣會在空氣中自燃,但本生仍能夠測量出銣的密度和熔點。1860年代所取得的密度值,與今天認可的數值只相差0.1 g/cm3,熔點值的偏差也在1 °C以內。[9]
科學家在1908年發現了銣的微放射性,但同位素理論在1910年代才被建立起來,加上放射性銣的半衰期超過1010年,所以當時對這一現象的解釋尤為困難。有關銣的衰變方式的爭論一直持續到1940年代末。目前已證實,87Rb會經β衰變成為穩定的87Sr。[10][11]
1920年代以前,銣還沒有工業用途。[12]此後,銣的最大應用在於化學和電子領域的科學研究和高新技術開發。1995年,埃里克·康奈爾、卡爾·埃德溫·威曼和沃爾夫岡·克特勒用銣-87實現了玻色–愛因斯坦凝聚,[13]並因此獲得了2001年的諾貝爾物理學獎。[14]
性質编辑
銣是一種質地非常柔軟、富延展性、可塑性高的銀白色金屬。[15]在所有非放射性鹼金屬元素中,銣的電正性排行第二。其熔點為39.3 °C。銣金屬會在水中劇烈反應,它會和汞產生汞齊,並且會和金、鐵、銫、鈉和鉀形成合金(但不會和鋰形成合金,儘管鋰和銣同屬鹼金屬[16])。與反應性稍低的鉀和反應性稍高的銫一樣,銣和水所產生的劇烈反應通常足以燃起所釋放出來的氫氣。它也可以在空氣中自燃。[15]銣的電離能很低,只有406 kJ/mol。[17]銣在焰色測試中會發出紫色,和鉀非常相似,所以要用到光譜學技術才能將兩者分辨開來。[來源請求]
化合物编辑

9O
2原子簇
氯化銣(RbCl)是最常用的銣化合物之一。在生物化學中,它可以用來促使細胞吸取DNA。由於生物體內的銣極少,且銣會被活細胞吸收而代替鉀,所以它能用作一種生物標記物。氫氧化銣(RbOH)具有腐蝕性,能作為大部份用到銣的化學反應的初始化合物。其他銣化合物還包括用在某些眼鏡鏡片中的碳酸銣(Rb2CO3),以及硫酸銣銅(Rb2SO4·CuSO4·6H2O)等。碘化銣銀(RbAg4I5)是所有已知離子晶體中,室溫電導率最高的。在製造薄膜電池時可以利用這一屬性。[18][19]
銣的氧化物有若干種,包括氧化銣(Rb2O)和Rb6O、Rb9O2等低氧化銣,后两种低氧化物可以在空气中燃烧。銣暴露在空氣中即會產生這些氧化物。在氧氣過剩的環境下,則會形成超氧化物(RbO2)。銣能和鹵素形成鹽,例如氟化銣、氯化銣、溴化銣及碘化銣等。[20]
同位素编辑
自然界中的銣元素由兩種同位素組成:穩定的85Rb(佔72.2%)以及長壽放射性同位素87Rb(佔27.8%),故銣是一種單一同位素元素(即只有一種穩定同位素)。[21]87Rb的存在使得自然界中的銣具有放射性,比活性約為670 Bq/g。這樣的輻射水平可以在110天內於照相底片上留下影像。[22][23]除85Rb和87Rb之外,還有30種人造的銣同位素,它們都具有放射性,且半衰期都在3個月以內。[24]
銣-87的半衰期為48.8×109年,這是宇宙年齡13.798×109年的三倍有餘。[25]它是一種原生核素,在地球形成時便已存在。在礦物中,銣常會代替鉀元素的位置,所以其分佈廣泛。87Rb在釋放一個負β粒子之後,會衰變成穩定的87Sr,這可以用於測定岩石的年齡。在地球內部的分級結晶過程中,鍶會集中在斜長石中,留下處於液態的銣。因此,在殘餘岩漿中銣對鍶的比例會隨時間增加,經活成分異作用形成銣/鍶比例較高的岩石。偉晶岩中的銣/鍶比例最高(10以上)。如果可以測得或推算出最初的鍶含量,那麼通過測量目前銣和鍶的含量以及87Sr/86Sr比例,就可以算出該岩石樣本的年齡。這一年齡只有在岩石不曾受變動的情況下才等於真實的年齡值。[26][27]
銣-82是銣的人造同位素之一,可經鍶-82的電子捕獲衰變過程產生,反應的半衰期為25.36天。銣-82會再經正電子發射衰變為穩定的氪-82,半衰期為76秒。[21]
存量编辑
銣在地球地殼中的豐度在所有元素中排第23位,與鋅相近,比銅更常見。[28]銣罕有獨立礦物,而是主要伴生在白榴石、銫榴石、光鹵石、鋰雲母和鐵鋰雲母等礦物之中,氧化銣大約佔這些礦物的1%。鋰雲母中的銣含量在0.3%和3.5%之間,是銣的主要商業來源。[29]某些含鉀礦物和氯化鉀都會含有不少的銣元素,有商業開採價值。[30]
銣在海水中的濃度平均為125 µg/L。相比之下,鉀的濃度則高得多(408 mg/L),銫則低得多(0.3 µg/L)。[31]铷是海水中第18丰富的元素。[32]
由於離子半徑較大,所以銣和更重的同族元素銫屬於所謂的「不相容成分」。[33]在熔岩結晶過程中,銣和銫聚集在一起,處於液態,是最後一個結晶的成分。因此,含有銣和銫的最大礦藏,都是經由這種濃縮過程所形成的偉晶岩礦帶。然而,由於銣會在結晶時代替鉀的位置,分散到各種含鉀礦物中,所以其濃縮、富集的程度遠低於銫,故富含銣的礦石非常罕見。從含有銫榴石的偉晶岩中可開採出銫,從鋰雲母中可開採出鋰,過程中也會產生銣作為副產品。[28]
銣的知名礦藏包括:位於加拿大曼尼托巴省伯尼克湖的富銣銫榴石礦藏,以及意大利厄爾巴島上的銣微斜長石((Rb,K)AlSi3O8)礦藏,其銣含量高達17.5%。[34]以上兩處同時也是銫的來源。[來源請求]
生產编辑
雖然銣在地殼中比銫更常見,但由於缺乏富銣礦物,加上其應用不廣,所以各種銣化合物的年產量只有2至4噸。[28]分離鉀、銣和銫的方法有若干種。對銣礬和銫礬重複進行分級結晶,30次以後便可獲得純銣礬。另外兩種方法分別利用氯錫酸鹽和亞鐵氫化物。[28][35]
1950至1960年代,鉀生產過程中一種稱為「Alkarb」的副產品曾經是銣元素的主要來源。Alkarb含21%的銣,其餘大部份是鉀,另有少量銫。[36]如今,銣是銫開採過程中的一种副產品,加拿大曼尼托巴省的銫榴石礦就是其中一例。[28]

應用编辑

由於銣和銫具有相似的物化性質和原子半徑,因此二者的下游應用類似,在多數領域中可以相互替代使用。[37]但由於銣產量較低、價格高昂,且銫具有比銣更強的電正性,使得大多數產業中銫產品的競爭力遠高於銣產品。
銣化合物有時會被添加在煙花當中,使它發出紫光。[38]銣可以用在磁流體發動機和熱傳導發電機中:高溫下形成的銣離子經過磁場,[39]作用就像發電機中的電樞,因而產生電流。用它製成的激光二極體價廉,且激光波長範圍適宜,維持高蒸氣壓所需的溫度也在中等範圍內,所以銣(特別是87Rb)是激光冷卻和玻色–愛因斯坦凝聚應用上最常用的一種原子。[40][41]
科學家曾用銣對3He進行極化,這樣產生的3He氣體擁有單一方向,而不是隨機方向的核自旋。激光對銣氣體進行光抽運,極化了的銣就會通過超精細交互作用使3He極化。[42]這樣自旋極化了的3He氣體可以用在中子極化測量中,或用於製造極化中子作其他用途。[43]
原子鐘的共振元件可以利用銣的能級的超精細結構,因此銣已被應用在高精度計時上。全球定位系統(GPS)常利用銣頻率標準來生成一個比銫頻率標準更精准、成本更低的「主頻率標準」。[44][45]這種銣頻率標準在電信工業中有大規模的生產。[46]
銣的其他潛在應用包括:蒸汽渦輪中的工作流體、真空管中的吸氣劑以及光度感應器元件等。[47]銣是一些特殊玻璃的成分,也可用於製造超氧化物。它能夠在細胞中代替鉀的位置,所以能被用來研究離子通道。銣氣體還被用於原子磁強計中。[48]科學家正在用87Rb,連同其他鹼金屬,來開發無自旋交換弛豫(SERF)原子磁強計。[48]
銣-82可用於正電子發射電腦斷層掃描。銣和鉀相似,所以含有大量鉀的生物組織也會積聚具放射性的銣元素。這一原理主要應用在心肌灌注成像。銣-82的半衰期只有76秒,所以必須從靠近病人的鍶-82衰變而得。[49]由於腦腫瘤的血腦屏障有所變異,所以腫瘤會比正常腦組織更容易積累銣。核醫學可以利用這一原理對腫瘤進行定位和照相。[50]
科學家曾做過實驗,以研究銣對患有躁鬱症和抑鬱症的病人有何影響。[51][52]透析治療期間患上抑鬱症的病人體內缺少銣,所以補充銣元素可能可以舒緩抑鬱症。[53]在某些試驗中,病人須連續60天攝入720 mg的氯化銣。[54][55]
安全编辑
| 铷 | |
|---|---|
 | |
| 危险性 | |
GHS危险性符号  | |
| GHS提示词 | Danger |
| H-术语 | H260, H314 |
| P-术语 | P223, P231+232, P280, P305+351+338, P370+378, P422[56] |
| NFPA 704 | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
銣金屬會和水發生劇烈的反應,甚至會爆炸;即使放在煤油中,也会缓慢反应,并被溶解的少量氧给氧化。因此,铷一般保存在真空安瓿或充有稀有气体(如氩气)的安瓿中。只要接觸到少許的空氣,包括滲入油中的氧氣,銣就會變成過氧化銣。因此它的安全措施和鉀金屬相似。[57]
與鈉和鉀一樣,銣溶在水中的時候幾乎永遠呈+1氧化態,在所有生物體內的銣也一樣。Rb+離子在人的體內似乎和鉀離子無異,所以主要積聚在細胞內液中。[58]銣離子並沒有明顯的毒性:一個70公斤重的人體內平均含有0.36克的銣,而在這一數值提升50甚至100倍之後,也沒有對試驗對象造成任何明顯的負面影響。[59]銣在人體內的生物半衰期為31至46天。[51]在老鼠身上進行的實驗指出,如果體內一小部份鉀替換成銣,身體是能夠承受的,但一旦肌肉組織內一半的鉀都換成銣,老鼠便會死亡。[60][61]
參考資料编辑
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ Haynes, William M. (编). CRC Handbook of Chemistry and Physics 92nd. Boca Raton, FL: CRC Press. 2011: 4.122. ISBN 1439855110.
- ^ Magnetic susceptibility of the elements and inorganic compounds 互联网档案馆的存檔,存档日期2012-01-12., in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ 谭彦妮; 刘咏. 铷及含铷材料的性能与应用研究进展 (PDF). 中国有色金属学报. 2017, 27 (2): 272–281 [2023-11-11]. (原始内容存档 (PDF)于2024-01-24).
- ^ 5.0 5.1 5.2 Kirchhoff,, G.; Bunsen, R. Chemische Analyse durch Spectralbeobachtungen. Annalen der Physik und Chemie. 1861, 189 (7): 337–381. Bibcode:1861AnP...189..337K. doi:10.1002/andp.18611890702.
- ^ 6.0 6.1 Weeks, Mary Elvira. The discovery of the elements. XIII. Some spectroscopic discoveries. Journal of Chemical Education. 1932, 9 (8): 1413–1434. Bibcode:1932JChEd...9.1413W. doi:10.1021/ed009p1413.
- ^ Ritter, Stephen K. C&EN: It's Elemental: The Periodic Table – Cesium. American Chemical Society. 2003 [2010-02-25]. (原始内容存档于2008-07-06).
- ^ Zsigmondy, Richard. Colloids and the Ultra Microscope. Read books. 2007: 69 [2010-09-26]. ISBN 978-1-4067-5938-9. (原始内容存档于2014-01-01).
- ^ Bunsen, R. Ueber die Darstellung und die Eigenschaften des Rubidiums. Annalen der Chemie und Pharmacie. 1863, 125 (3): 367. doi:10.1002/jlac.18631250314.
- ^ Lewis, G.M. The natural radioactivity of rubidium. Philosophical Magazine Series 7. 1952, 43 (345): 1070–1074. doi:10.1080/14786441008520248.
- ^ Campbell, N. R.; Wood, A. The Radioactivity of Rubidium. Proceedings of the Cambridge Philosophical Society. 1908, 14: 15.
- ^ Butterman, W.C.; Reese, Jr., R.G. Mineral Commodity Profiles Rubidium (PDF). United States Geological Survey. [2010-10-13]. (原始内容存档 (PDF)于2011-09-25).
- ^ Press Release: The 2001 Nobel Prize in Physics. [2010-02-01]. (原始内容存档于2009-08-30).
- ^ Levi, Barbara Goss. Cornell, Ketterle, and Wieman Share Nobel Prize for Bose-Einstein Condensates. Physics Today (Physics Today online year = 2001): 14. Bibcode:2001PhT....54l..14L. doi:10.1063/1.1445529.
- ^ 15.0 15.1 Ohly, Julius. Rubidium. Analysis, detection and commercial value of the rare metals. Mining Science Pub. Co. 1910.
- ^ Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils. Vergleichende Übersicht über die Gruppe der Alkalimetalle. Lehrbuch der Anorganischen Chemie 91–100. Walter de Gruyter. 1985: 953–955. ISBN 978-3-11-007511-3 (德语).
- ^ Moore, John W; Stanitski, Conrad L; Jurs, Peter C. Principles of Chemistry: The Molecular Science. 2009: 259 [2014-12-17]. ISBN 978-0-495-39079-4. (原始内容存档于2013-10-13).
- ^ Smart, Lesley; Moore, Elaine. RbAg4I5. Solid state chemistry: an introduction. CRC Press. 1995: 176–177. ISBN 978-0-7487-4068-0.
- ^ Bradley, J. N.; Greene, P. D. Relationship of structure and ionic mobility in solid MAg4I5. Trans. Faraday Soc. 1967, 63: 2516. doi:10.1039/TF9676302516.
- ^ Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英语).
- ^ 21.0 21.1 Audi, Georges; Bersillon, O.; Blachot, J.; Wapstra, A.H. The NUBASE Evaluation of Nuclear and Decay Properties. Nuclear Physics A (Atomic Mass Data Center). 2003, 729 (1): 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Strong, W. W. On the Possible Radioactivity of Erbium, Potassium and Rubidium. Physical Review. Series I. 1909, 29 (2): 170–173. Bibcode:1909PhRvI..29..170S. doi:10.1103/PhysRevSeriesI.29.170.
- ^ Lide, David R; Frederikse, H. P. R. CRC handbook of chemistry and physics: a ready-reference book of chemical and physical data. June 1995: 4–25 [2014-12-17]. ISBN 978-0-8493-0476-7. (原始内容存档于2013-11-03).
- ^ Universal Nuclide Chart
 . nucleonica. [2017-01-03]. (原始内容存档于2017-02-19).
. nucleonica. [2017-01-03]. (原始内容存档于2017-02-19). - ^ Planck collaboration; Ade, P. A. R.; Aghanim, N.; Armitage-Caplan, C.; Arnaud, M.; Ashdown, M.; Atrio-Barandela, F.; Aumont, J.; et al. Planck 2013 results. XVI. Cosmological parameters. Submitted to Astronomy & Astrophysics. 2013, 1303: 5076. Bibcode:2014A&A...571A..16P. arXiv:1303.5076
 . doi:10.1051/0004-6361/201321591.
. doi:10.1051/0004-6361/201321591. - ^ Attendorn, H. -G.; Bowen, Robert. Rubidium-Strontium Dating. Isotopes in the Earth Sciences. Springer. 1988: 162–165. ISBN 978-0-412-53710-3.
- ^ Walther, John Victor. Rubidium-Strontium Systematics. Essentials of geochemistry. Jones & Bartlett Learning. 1988 2009: 383–385. ISBN 978-0-7637-5922-3.
- ^ 28.0 28.1 28.2 28.3 28.4 Butterman, William C.; Brooks, William E.; Reese, Jr., Robert G. Mineral Commodity Profile: Rubidium (PDF). United States Geological Survey. 2003 [2010-12-04]. (原始内容存档 (PDF)于2011-09-25).
- ^ Wise, M. A. Trace element chemistry of lithium-rich micas from rare-element granitic pegmatites. Mineralogy and Petrology. 1995, 55 (13): 203–215. Bibcode:1995MinPe..55..203W. doi:10.1007/BF01162588.
- ^ Norton, J. J. Lithium, cesium, and rubidium—The rare alkali metals. Brobst, D. A., and Pratt, W. P. (编). United States mineral resources. Paper 820. U.S. Geological Survey Professional. 1973: 365–378 [2010-09-26]. (原始内容存档于2010-07-21).
- ^ Bolter, E; Turekian, K; Schutz, D. The distribution of rubidium, cesium and barium in the oceans. Geochimica et Cosmochimica Acta. 1964, 28 (9): 1459. Bibcode:1964GeCoA..28.1459B. doi:10.1016/0016-7037(64)90161-9.
- ^ William A. Hart |title=The Chemistry of Lithium, Sodium, Potassium, Rubidium, Caesium, and Francium |page=371
- ^ McSween, Harry Y; Jr,; Huss, Gary R. Cosmochemistry. 2010: 224 [2014-12-17]. ISBN 978-0-521-87862-3. (原始内容存档于2013-12-13).
- ^ Teertstra, David K.; Cerny, Petr; Hawthorne, Frank C.; Pier, Julie; Wang, Lu-Min; Ewing, Rodney C. Rubicline, a new feldspar from San Piero in Campo, Elba, Italy. American Mineralogist. 1998, 83 (11–12 Part 1): 1335–1339 [2014-12-17]. (原始内容存档于2011-09-28).
- ^ bulletin 585. United States. Bureau of Mines. 1995.
- ^ Cesium and Rubidium Hit Market. Chemical & Engineering News. 1959, 37 (22): 50. doi:10.1021/cen-v037n022.p050.
- ^ 王酉臣; 王登红. 铷——战略性新兴资源中的宠儿. 自然资源科普与文化. 2020, 1: 12–15 [2023-11-11]. (原始内容存档于2023-11-11).
- ^ Koch, E.-C. Special Materials in Pyrotechnics, Part II: Application of Caesium and Rubidium Compounds in Pyrotechnics. Journal Pyrotechnics. 2002, 15: 9–24 [2014-12-17]. (原始内容存档于2011-07-13).
- ^ Boikess, Robert S; Edelson, Edward. Chemical principles. 1981: 193. ISBN 978-0-06-040808-4.
- ^ Eric Cornell; et al. Bose-Einstein condensation (all 20 articles) 101. 1996: 419–618. doi:10.6028/jres.101.045. (原始内容存档于2011-10-14).
|journal=被忽略 (帮助);|issue=被忽略 (帮助) - ^ Martin, J L; McKenzie, C R; Thomas, N R; Sharpe, J C; Warrington, D M; Manson, P J; Sandle, W J; Wilson, A C. Output coupling of a Bose-Einstein condensate formed in a TOP trap. Journal of Physics B: Atomic, Molecular and Optical Physics. 1999, 32 (12): 3065. Bibcode:1999JPhB...32.3065M. arXiv:cond-mat/9904007
 . doi:10.1088/0953-4075/32/12/322.
. doi:10.1088/0953-4075/32/12/322. - ^ Gentile, T. R.; Chen, W. C.; Jones, G. L.; Babcock, E.; Walker, T. G. Polarized 3He spin filters for slow neutron physics (PDF). Journal of Research of the National Institute of Standards and Technology: 299–304. (原始内容 (PDF)存档于2011年10月18日).
- ^ Neutron spin filters based on polarized helium-3. NIST Center for Neutron Research 2002 Annual Report. [2008-01-11]. (原始内容存档于2007-05-20).
- ^ Eidson, John C. GPS. Measurement, control, and communication using IEEE 1588. 2006-04-11: 32 [2014-12-17]. ISBN 978-1-84628-250-8. (原始内容存档于2013-06-02).
- ^ King, Tim; Newson, Dave. Rubidium and crystal oscillators. Data network engineering. 1999-07-31: 300 [2014-12-17]. ISBN 978-0-7923-8594-3. (原始内容存档于2013-06-02).
- ^ Marton, L. Rubidium Vapor Cell. Advances in electronics and electron physics. 1977-01-01 [2014-12-17]. ISBN 978-0-12-014644-4. (原始内容存档于2013-06-02).
- ^ Mittal. Introduction To Nuclear And Particle Physics. 2009: 274. ISBN 978-81-203-3610-0.
- ^ 48.0 48.1 Li, Zhimin; Wakai, Ronald T.; Walker, Thad G. Parametric modulation of an atomic magnetometer. Applied Physics Letters. 2006, 89 (13): 134105. Bibcode:2006ApPhL..89m4105L. doi:10.1063/1.2357553.
- ^ Jadvar, H.; Anthony Parker, J. Rubidium-82. Clinical PET and PET/CT. 2005: 59. ISBN 978-1-85233-838-1.
- ^ Yen, CK; Yano, Y; Budinger, TF; Friedland, RP; Derenzo, SE; Huesman, RH; O'Brien, HA. Brain tumor evaluation using Rb-82 and positron emission tomography. Journal of Nuclear Medicine. 1982, 23 (6): 532–7. PMID 6281406.
- ^ 51.0 51.1 Paschalis, C; Jenner, F A; Lee, C R. Effects of rubidium chloride on the course of manic-depressive illness. J R Soc Med. 1978, 71 (9): 343–352. PMC 1436619
 . PMID 349155.
. PMID 349155. - ^ Malekahmadi, P; Williams, John A. Rubidium in psychiatry: Research implications. Pharmacology Biochemistry and Behavior. 1984, 21: 49. doi:10.1016/0091-3057(84)90162-X.
- ^ Canavese, Caterina; Decostanzi, Ester; Branciforte, Lino; Caropreso, Antonio; Nonnato, Antonello; Sabbioni, Enrico. Depression in dialysis patients: Rubidium supplementation before other drugs and encouragement?. Kidney International. 2001, 60 (3): 1201–1201. doi:10.1046/j.1523-1755.2001.0600031201.x.
- ^ Lake, James A. Textbook of Integrative Mental Health Care. New York: Thieme Medical Publishers. 2006: 164–165. ISBN 1-58890-299-4.
- ^ Torta, R; Ala, G; Borio, R; Cicolin, A; Costamagna, S; Fiori, L; Ravizza, L. Rubidium chloride in the treatment of major depression. Minerva psichiatrica. 1993, 34 (2): 101–10. PMID 8412574.
- ^ https://www.sigmaaldrich.com/catalog/product/aldrich/276332?lang=en®ion=US
- ^ Martel, Bernard; Cassidy, Keith. Rubidium. Chemical risk analysis: a practical handbook. 2004-07-01: 215 [2014-12-17]. ISBN 978-1-903996-65-2. (原始内容存档于2013-06-02).
- ^ Relman, AS. The Physiological Behavior of Rubidium and Cesium in Relation to That of Potassium. The Yale journal of biology and medicine. 1956, 29 (3): 248–62. PMC 2603856
 . PMID 13409924.
. PMID 13409924. - ^ Fieve, Ronald R.; Meltzer, Herbert L.; Taylor, Reginald M. Rubidium chloride ingestion by volunteer subjects: Initial experience. Psychopharmacologia. 1971, 20 (4): 307–14. PMID 5561654. doi:10.1007/BF00403562.
- ^ Meltzer, HL. A pharmacokinetic analysis of long-term administration of rubidium chloride. Journal of clinical pharmacology. 1991, 31 (2): 179–84. PMID 2010564. doi:10.1002/j.1552-4604.1991.tb03704.x. (原始内容存档于2012-07-09).
- ^ Follis, Richard H., Jr. Histological Effects in rats resulting from adding Rubidium or Cesium to a diet deficient in potassium. AJP – Legacy. 1943, 138 (2): 246. (原始内容存档于2012-07-11).
延伸閱讀编辑
- Meites, Louis (1963). Handbook of Analytical Chemistry (New York: McGraw-Hill Book Company, 1963)
- Steck, Daniel A. Rubidium-87 D Line Data (PDF). Los Alamos National Laboratory (technical report LA-UR-03-8638). [2014-12-17]. (原始内容 (PDF)存档于2013-11-02).
外部連結编辑
- 元素铷在洛斯阿拉莫斯国家实验室的介紹(英文)
- EnvironmentalChemistry.com —— 铷(英文)
- 元素铷在The Periodic Table of Videos(諾丁漢大學)的介紹(英文)
- 元素铷在Peter van der Krogt elements site的介紹(英文)
- WebElements.com – 铷(英文)
- Rubidium (页面存档备份,存于互联网档案馆) at The Periodic Table of Videos(諾丁漢大學)